Nadtlenki organiczne
17 Lutego 2023Nadtlenki organiczne należą do tych grup związków chemicznych, których niekontrolowane uwolnienie może być przyczyną trudnego do przewidzenia ciągu reakcji chemicznych. Do zapłonu dochodziło w tak prozaicznych wypadkach, jak zamiatanie rozsypanego nadtlenku słomianą miotłą czy też wzajemne tarcie kryształków substancji w pojemniku - zdarzało się to np. dla nadtlenku benzoilu [1].
Pilnej uwagi wymaga dobór sorbentów wykorzystywanych do zbierania rozlewisk ciekłych nadtlenków lub ich roztworów. W niektórych przypadkach stosowanie sorbentów na bazie organicznej (np. trocin) może skończyć się niespodziewanym zapłonem. Pożar tych związków cechuje się znacznie wyższą intensywnością, związaną z obecnością nietrwałego wiązania nadtlenkowego. W pożarze nadtlenku wytworzą się wyraźnie większe płomienie niż w przypadku standardowych paliw węglowodorowych na takiej samej powierzchni. Konsekwencją wysokiej intensywności spalania może być rozbryzg palącej się substancji. .png?1683553654858) Część nadtlenków w stanie czystym (jak np. nadtlenek benzoilu) eksploduje w kontakcie z płomieniem. Takiego ryzyka nie da się uniknąć mimo stosowania różnego rodzaju odczulaczy. W warunkach pożarowych oddziaływanie strumienia ciepła może w niesprzyjających okolicznościach uwolnienia substancji doprowadzić do odparowania odczulacza, jeśli jest nim np. woda. Co ciekawe, wspomniany suchy nadtlenek benzoilu ulega zapłonowi znacznie łatwiej niż proch czarny.
Część nadtlenków w stanie czystym (jak np. nadtlenek benzoilu) eksploduje w kontakcie z płomieniem. Takiego ryzyka nie da się uniknąć mimo stosowania różnego rodzaju odczulaczy. W warunkach pożarowych oddziaływanie strumienia ciepła może w niesprzyjających okolicznościach uwolnienia substancji doprowadzić do odparowania odczulacza, jeśli jest nim np. woda. Co ciekawe, wspomniany suchy nadtlenek benzoilu ulega zapłonowi znacznie łatwiej niż proch czarny.
W przypadku nadtlenków organicznych odczulanych rozcieńczalnikami organicznymi pożar może doprowadzić do wypalenia się rozcieńczalnika. Objawia się to nagłym zintensyfikowaniem procesu spalania.
O nadtlenkach organicznych w ratownictwie mówi się niewiele. Do ich uwolnienia w ilościach wymagających interwencji jednostek PSP dochodzi dość rzadko, a informacje o zdarzeniach na terenie zakładów przemysłowych w niewielkim stopniu wypływają na zewnątrz. Inną kwestią jest dość rozbudowana struktura form przewozu, mająca na celu zmniejszenie zagrożenie związanego z tymi substancjami. Struktura ta nie jest łatwa do odczytania dla ratowników. Podczas prowadzenia działań rozpoznawczych z dystansu nie zidentyfikujemy łatwo konkretnej substancji na podstawie numeru UN. Określimy jedynie podstawowe zagrożenia wynikłe z piktogramów. Brak wiedzy na podstawowym etapie rozpoznania może mieć poważne konsekwencje. Znane są przypadki, gdy doszło w ten sposób do poważnych zdarzeń, pociągających za sobą śmierć wielu ratowników. Było tak np. w Tokio, gdzie śmierć podczas wybuchu 3600 kg nadtlenku ketonu metylowo-etylowego poniosło
19 ratowników. Warto więc zdobyć podstawową wiedzę na temat tej grupy związków - nie jest do tego konieczne głębsze wnikanie w meandry chemii.
Co to są nadtlenki organiczne
Nadtlenki są pochodną nadtlenku wodoru H2O2 (H-O-O-H), zawierają w swojej strukturze wiązanie nadtlenkowe -O-O-. W przypadku nadtlenków organicznych można wyróżnić dwie zasadnicze grupy. Pierwsza z nich to hydronadtlenki mające podstawiony rodnik organiczny (R-) zamiast jednego atomu wodoru (R-O-O-H). Prostym przykładem takiego związku może być np. hydronadtlenek metylu CH3-O-O-H.
Drugą grupę nadtlenków organicznych stanowią związki, w których obydwa atomy wodoru w H2O2 zostały podstawione rodnikami organicznymi. Ich ogólna struktura to R1-O-O-R2, przy czym w szczególnych przypadkach grupa R1 i R2 jest taka sama. Przykładem może tu być nadtlenek dimetylu CH3-O-O-CH3.
Nadtlenki organiczne wykorzystuje się najczęściej jako inicjatory reakcji łańcuchowych. Nazywane są także utwardzaczami lub też substancjami sieciującymi. Są wykorzystywane do produkcji szerokiej gamy tworzyw sztucznych, takich jak poliakrylany, poliestry, żywice epoksydowe, polietylen, polipropylen, polistyren, silikony itp.
Kategorie transportowe nadtlenków organicznych
Nadtlenki organiczne mają wyodrębnioną klasę w transporcie materiałów niebezpiecznych - 5.2. W jej obrębie występuje podział na dwie grupy: nadtlenki organiczne niewymagające kontroli temperatury (P1) oraz jej wymagające (P2). Nie każda mieszanina lub roztwór zawierająca nadtlenki będzie włączana do klasy 5.2. Dzieje się tak w dwóch przypadkach: gdy w składzie nie znajduje się więcej niż 1% tlenu aktywnego pochodzącego z nadtlenków organicznych, przy zawartości nadtlenku wodoru (H2O2) nieprzekraczającej 1%, lub gdy zawartość tlenu aktywnego pochodząca z nadtlenku organicznego nie przekracza 0,5%, a stężenie H2O2 mieści się w przedziale 1% < c < 7%.
Warto zwrócić uwagę, że w celach obliczeniowych w cząsteczce nadtlenku jedynie jeden atom tlenu grupy nadtlenkowej -O-O- uważany jest za aktywny. Stąd też zawartość tlenu aktywnego pochodzącą z nadtlenków organicznych można wyrazić wzorem:
![]()
ni - liczba grup nadtlenkowych w danym nadtlenku organicznym
ci - stężenie danego nadtlenku organicznego wyrażone w % masowych
Mi - masa molowa danego nadtlenku organicznego
Suma w niniejszym wzorze oznacza, że może być on wykorzystany także do liczenia zawartości tlenu aktywnego w mieszaninie zawierającej więcej niż jeden typ nadtlenku organicznego.
Nadtlenki organiczne zaklasyfikowane zostały do siedmiu typów, biorąc pod uwagę stopień stwarzanego przez nie zagrożenia. Typy oznacza się literowo od A do G. Jeżeli nadtlenek organiczny zostanie przypisany do najbardziej niebezpiecznej kategorii (A), nie jest on dopuszczony do przewozu w opakowaniu, w którym został zbadany. Najbardziej rozcieńczone formulacje nadtlenków zaliczane są zaś do typu G. Z racji stwarzania najmniejszego zagrożenia nie podlegają one przepisom klasy 5.2. Klasyfikacja typów nadtlenków organicznych od B do F powiązana jest bezpośrednio z maksymalną ilością materiału dopuszczoną dla jednej sztuki przesyłki.
Rozcieńczyć, by przetransportować
Aby zapewnić bezpieczny przewóz nadtlenków organicznych, w wielu przypadkach stosuje się ich odczulanie. Polega ono na ich rozcieńczaniu za pomocą ciekłych lub stałych materiałów organicznych, stałych materiałów nieorganicznych lub też zwilżaniu/rozcieńczaniu wodą. Jeżeli forma stężenia procentowego substancji nie jest określona, to powinno się ją rozumieć jako wyrażoną w procentach masowych, zaokrąglonych do najbliższej liczby całkowitej. Zasadą jest przeprowadzenie procesu odczulania tak, aby w razie niekontrolowanego uwolnienia substancji stężenie nadtlenku organicznego nie osiągnęło poziomu niebezpiecznego.
Do odczulania stosuje się dwa typy rozcieńczalników organicznych, oznaczanych jako A oraz B. Typ A stanowią ciekłe materiały organiczne, zgodne z nadtlenkiem organicznym, o temperaturze wrzenia nie niższej niż 150°C. Rozcieńczalniki typu A jako bezpieczniejsze pożarowo mogą być stosowane do odczulania wszystkich nadtlenków organicznych.
Rozcieńczalniki typu B są ciekłymi materiałami organicznymi, zgodnymi z nadtlenkami organicznymi, mającymi temperaturę wrzenia niższą niż 150°C, ale nie mniejszą niż 60°C. Rozcieńczalniki typu B muszą mieć temperaturę zapłonu nie niższą niż 5°C. Mogą zostać zastosowane do odczulania wszystkich nadtlenków organicznych, pod warunkiem, że temperatura wrzenia materiału ciekłego jest co najmniej o 60°C wyższa niż temperatura samoprzyspieszającego się rozkładu nadtlenku organicznego (TSR) w sztuce przesyłki o masie 50 kg. Zbyt niska temperatura wrzenia rozcieńczalnika w warunkach oddziaływania zewnętrznego źródła ciepła na uszkodzoną sztukę materiału transportowanego lub magazynowanego mogłaby spowodować szybsze jego parowanie w porównaniu do rozpuszczonego w nim nadtlenku. To skutkowałoby zatężeniem nadtlenku i wzrostem zagrożenia ze strony substancji.
Temperatura pod nadzorem
Część przewożonych formulacji nadtlenków organicznych wymaga kontroli temperatury podczas przewozu. Temperatura kontrolowana to najwyższa temperatura, w której przewóz danego materiału może odbywać się w sposób bezpieczny. Dla klasy 5.2 warunek ten dotyczy materiałów oznaczonych numerami UN 3111-3120. W przypadku UN 3535, a więc przedmiotów zawierających nadtlenek organiczny I.N.O, materiał może należeć zarówno do substancji wymagających, jak i niewymagających kontroli temperatury. W przypadku formulacji oznaczonych numerem UN 3101-3010 kontrola nie będzie konieczna. 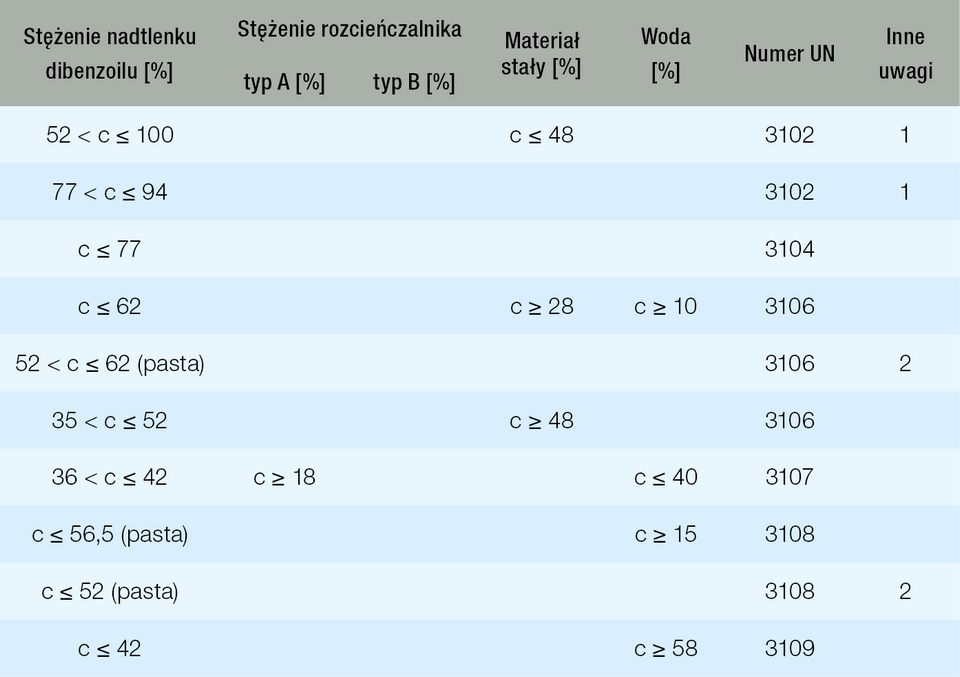 Utrata możliwości kontroli temperatury wiąże się z koniecznością wdrożenia postępowania awaryjnego po osiągnięciu temperatury awaryjnej. Realna temperatura przewozu materiałów jest często niższa niż temperatura kontrolowana. Nie może ona jednak być zbyt niska, by nie doprowadzić do rozdziału faz w transportowanym materiale.
Utrata możliwości kontroli temperatury wiąże się z koniecznością wdrożenia postępowania awaryjnego po osiągnięciu temperatury awaryjnej. Realna temperatura przewozu materiałów jest często niższa niż temperatura kontrolowana. Nie może ona jednak być zbyt niska, by nie doprowadzić do rozdziału faz w transportowanym materiale.
Zastosowany rozcieńczalnik może mieć wpływ na to, czy dana formulacja będzie wymagała kontroli temperatury, czy też nie. Na przykład dla nadtlenku di-2,4-(dichlorobenzoilu) zwilżonego wodą przy jego stężeniu c ≤ 77% kontrola temperatury nie jest obligatoryjna. Jeżeli jednak jego stężenie okaże się mniejsze (c ≤ 52%), ale substancja będzie transportowana w postaci pasty niezawierającej oleju silikonowego, kontrola to konieczność (Tkontr = 20oC). Obecność oleju silikonowego w paście sprawi z kolei, że monitorowanie temperatury będzie zbędne.
Dany nadtlenek organiczny, w zależności od składu, zastosowanych rozcieńczalników czy też stanu skupienia, może mieć różny numer UN. Klasa nadtlenków organicznych jest jednak w swojej strukturze wyjątkowo rozbudowana. Na przykład popularnie wykorzystywany nadtlenek benzoilu (nadtlenek dibenzoilu) może być obecny w formulacji zarówno pod numerem 3102, 3104, jak i pod numerami 3106-3109 (tabela). Należy jednak pamiętać, że numery UN przyporządkowane nadtlenkom organicznym mają charakter ogólny i nie są przypisane konkretnym substancjom. Np. pod numerem UN 3102 kryje się nadtlenek organiczny typu B stały, niewymagający kontroli temperatury, a więc dowolna formulacja spełniająca te kryteria. Może to znacznie utrudnić rozpoznanie wstępne w przypadku zdarzeń podczas transportu nadtlenków organicznych.
Nadtlenki organiczne poza kontrolą
Scenariusz z horroru: Nowa Anglia, kwiecień 1962 r.
Zdarzenie dowodzące niebezpiecznych właściwości nadtlenków organicznych miało miejsce na terenie magazynu firmy zajmującej się produkcją materiałów skórzanych. Na naczepie rozładowywanego tira o szerokości 2,4 m, długości 12 m i wysokości 3 m znajdowało się
18,5 t nadtlenków organicznych: nadtlenek ketonu metylowo-etylowego w 18 kg beczkach i 3,6 kg pojemnikach polietylenowych; mokry i suchy nadtlenek benzoilu w polietylenowych torbach owiniętych papierem o wadze 0,45 kg; nadtlenek lauroilu w 45 kg beczkach oraz wodoronadtlenek t-butylu w 15,9 kg beczkach.
Kierowca i pracownicy magazynu podczas rozładunku zauważyli wydobywający się z przedniej części naczepy jasny dym przypominający mgłę, o zapachu palącego się papieru. Na miejsce zostali wezwani strażacy. Rozłożyli linie wężowe - obok przyczepy oraz z tyłu, na platformie ładunkowej. Prowadząc działania w obronie, pięciu strażaków skryło się za betonową ścianą oporową o wysokości 1,2 m. Stąd mogli bezpośrednio podawać prąd gaśniczy na otwarty tył ciężarówki.
W pewnym momencie przyczepę, w której rozwijał się stosunkowo niewielki pożar, rozerwał nagły wybuch. Jak relacjonował świadek - „okolica pokryła się deszczem płomieni”.
Drewniane budynki magazynowe zostały zmiecione siłą wybuchu, a ich pozostałości stanęły w płomieniach. Trzech z pięciu strażaków kryjących się za ścianą spłonęło żywcem, dwóch pozostałych, których siła wybuchu wyrzuciła w kałużę błota, zostało poparzonych. Intensywność pożaru uniemożliwiła udzielenie im pomocy na 30 min. Do tego momentu chronili się przed pożarem, przeciągając na siebie stalową blachę oraz zwilżając wodą ubrania i skórę.
Zginął także ratownik stojący przy drugim pojeździe, a strażak, który wcześniej obsługiwał hydrant, został poważnie ranny.
Przyczyny zapłonu nie zostały jednoznacznie ustalone. Mógł być spowodowany wstrząsami podczas transportu i wynikającymi z nich wzajemnymi tarciami przesuwających się kartonów. Nie jest wykluczone, że zewnętrzne części opakowań były zanieczyszczone śladami nadtlenków. Nadtlenek benzoilu znajdujący się w masie ładunkowej jest bardzo podatny na zapłon i wybuch w stanie suchym. Zgodnie z ówczesnymi wymaganiami transportowymi mógł być przewożony w formie suchej w papierowych torbach o wadze 0,45 kg (jednego funta), z wewnętrzną okładziną polietylenową. Torby te powinny być umieszczane w skrzyniach ochronnych.
Biorąc pod uwagę współczesne wymogi, suchy nadtlenek benzoilu stanowiłby nadtlenek organiczny typu A, podlegający regulacjom dla materiałów wybuchowych, a więc nie byłby dopuszczony do przewozu jako materiał klasy 5.2.
Latająca suszarka. Ohio, styczeń 2002 r.
Do ciekawego zdarzenia doszło w Catalyst Systems Inc. w Gnadenhutten w stanie Ohio. Wybuchowemu rozkładowi w suszarce próżniowej uległo około 90 kg nadtlenku benzoilu (BPO). Niekontrolowany przebieg reakcji chemicznej nastąpił podczas procesu suszenia substancji, co miało doprowadzić do uzyskania jej o czystości 98%.
Siła eksplozji wyrzuciła ciężką suszarkę, która przebiła się przez ścianę, powodując rozległe uszkodzenia budynku. O niebywałym szczęściu może mówić kilku pracowników jedzących lunch w tym samym pomieszczeniu, zaledwie 10 m dalej w. Jednego z pracowników trafił odłamek.
Co ciekawe, śledczy Amerykańskiej Rady Bezpieczeństwa Chemicznego (CSB) nie byli w stanie określić zdarzenia inicjującego, które doprowadziło do egzotermicznego rozpadu substancji. Jednakże dochodzenie bezsprzecznie wykazało, że kierownictwo zakładu nie wprowadziło odpowiedniego systemu identyfikacji zagrożeń. Kupiono używaną suszarkę, bez załączonego schematu elektrycznego ani rysunków technicznych. Nie opracowano pisemnych procedur operacyjnych dotyczących suszenia chemikaliów - operatorzy otrzymali jedynie ustne instrukcje postępowania.
W polskich warunkach obecność nadtlenków w przemyśle regulowana jest między innymi Rozporządzeniem ministra przemysłu i handlu z dnia 1 marca 1995 r. w sprawie bezpieczeństwa i higieny pracy przy produkcji, stosowaniu, magazynowaniu i transporcie wewnątrzzakładowym nadtlenków organicznych. W branży przemysłowej uważa się, że wymaga ono głębokiej nowelizacji.
Wybuch w laboratorium: San Francisco, marzec 1995 r. Nadtlenki potrafią zaskoczyć nie tylko wtedy, gdy jesteśmy świadomi ich obecności. Czasami tworzą się w miejscach, w których się ich nie spodziewamy. Potrafią być niespodzianką nawet dla personelu laboratoriów chemicznych. Tak jest choćby w przypadku eterów, w tym popularnego eteru dietylowego. Jego właściwości: palność i wybuchowość, wynikające między innymi z bardzo wysokiej prężności par, są powszechnie znane. Gorzej natomiast ze świadomością, że eter dietylowy tworzy szeroką gamę nadtlenków organicznych na skutek wolnorodnikowej reakcji z tlenem z powietrza. Mimo dodawania inhibitorów długo przetrzymywany eter może zawierać ich sporą ilość.
Nadtlenki potrafią zaskoczyć nie tylko wtedy, gdy jesteśmy świadomi ich obecności. Czasami tworzą się w miejscach, w których się ich nie spodziewamy. Potrafią być niespodzianką nawet dla personelu laboratoriów chemicznych. Tak jest choćby w przypadku eterów, w tym popularnego eteru dietylowego. Jego właściwości: palność i wybuchowość, wynikające między innymi z bardzo wysokiej prężności par, są powszechnie znane. Gorzej natomiast ze świadomością, że eter dietylowy tworzy szeroką gamę nadtlenków organicznych na skutek wolnorodnikowej reakcji z tlenem z powietrza. Mimo dodawania inhibitorów długo przetrzymywany eter może zawierać ich sporą ilość.
Tworzący się hydronadtlenek eteru dietylowego to ciecz, która rozpuszcza się w eterze. Po dłuższym czasie tworzy się natomiast stały polimer koloru białego, którego obecności możemy się spodziewać w górnej części butelki, tuż pod korkiem. Polinadtlenek eteru dietylowego jest ekstremalnie wrażliwy i może wybuchnąć sam z siebie czy też podczas przenoszenia butelki. Nadtlenku będzie się tworzyło tym więcej, im więcej kontaktu ze światłem słonecznym ma eter, czyli np. wtedy, gdy będzie przechowywany w miejscach z dużą ilością światła dziennego, w przezroczystych butelkach.
Do ciekawego zdarzenia doszło w laboratorium profesora Martina Shetlara z University of California San Francisco 9 marca 1995 r. Tego dnia brał on udział w rutynowym sprzątaniu laboratorium, opróżniając szafki ze starych chemikaliów, które miały zostać usunięte jako odpady chemiczne.
W tylnej części szafki natknął się na dwie butelki eteru, które stały w niej od około 10 lat. Świadomy niebezpieczeństwa Shetlar ostrożnie ustawił je w dygestorium obok szafki, następnie oddalił się od tego miejsca. Po pewnej chwili usłyszał trzask. Kiedy odwrócił się, aby zobaczyć, co spowodowało ten dźwięk, nastąpiła eksplozja, w wyniku której został ranny. Wybuch był na tyle silny, że zniszczył dwanaście okien.
Postępowanie podczas działań ratowniczych
Nieco informacji dotyczących postępowania w zdarzeniach z udziałem nadtlenków organicznych możemy znaleźć w publikacji „Zasady postępowania ratowniczego 2016”, opracowanej na zlecenie GIOŚ na podstawie „The 2016 Emergency Guide Book”. W książce zawarto trzy procedury, o numerach 145, 146 i 148, zatytułowane odpowiednio: „Nadtlenki organiczne (wrażliwe na działanie wysokiej temperatury i zanieczyszczeń)”, „Nadtlenki organiczne (wrażliwe na działanie wysokiej temperatury, zanieczyszczeń i tarcia)”, „Nadtlenki organiczne (wrażliwe na działanie wysokiej temperatury i zanieczyszczenia. Temperatura kontrolowana)”.
Biorąc pod uwagę zdarzenia, do których doszło w przeszłości, całkowicie zasadne wydają się znaczne wielkości strefy ewakuacji, w przypadku wycieku - 250 m, w przypadku zagrożenia pożarem zbiornika magazynowego lub cysterny - 800 m. Podobnie rzecz się ma się, jeśli chodzi o izolację strefy uwolnienia - powinna ona wynosić 50 m dla cieczy i 25 m dla ciał stałych.
Warto również zwrócić uwagę na informację dotyczącą konieczności utrzymania substancji w stanie wilgotnym. Zroszenie materiału prądem mgłowym eliminuje źródła zapłonu elektryczności statycznej, zmniejsza ryzyko tarcia, a także redukuje ryzyko przekroczenia temperatury samoprzyspieszającego się rozkładu (TSR), która dla części nadtlenków jest stosunkowo niska. Na przykład dla naddiwęglanu diizopropylu wynosi ona zaledwie +12oC.
Zraszanie wodą lub też zabezpieczenie warstwą piany ciężkiej jest szczególnie istotne, zwłaszcza w przypadku oddziaływania zewnętrznych źródeł ciepła. Nawet stosunkowo stabilne i bezpieczne nadtlenki organiczne mają relatywnie łatwe do przekroczenia wartości TSR. Np. dla nadtlenku dikumylu, będącego nadtlenkiem stałym typu F, niewymagającego kontroli temperatury podczas przewozu, TSR wynosi zaledwie +120oC. Należy pamiętać, że niektóre rozlewiska ciekłych formulacji nadtlenków mogą wymagać pian alkoholoodpornych.
Likwidacja źródeł tarcia przez zwilżanie jest ważna przede wszystkim dla stałych nadtlenków organicznych wymagających kontroli temperatury. Oznaczono je następującymi numerami UN (uporządkowanymi w kolejności malejącego ryzyka): 3112, 3114, 3116, 3118, 3120.
Do sorbowania ciekłych nadtlenków organicznych powinno się bezwzględnie wykorzystywać niepalne sorbenty nieorganiczne, o ile są kompatybilne. Zastosowanie sorbentów bazujących na materiale organicznym, np. tych na bazie torfu, trocin, polipropylenu lub innych niekompatybilnych substancji, może spowodować samonagrzewanie, w konsekwencji przekroczenie temperatury TSR i w dalszej kolejności zapłon. W przypadku nadtlenków organicznych kompatybilność sorbentu mineralnego warto sprawdzić na małej próbce pobranego materiału, z wykorzystaniem kamery termowizyjnej. Pomocna w ocenie może być też strona https://cameochemicals.noaa.gov. Pozwala ona wyszukać substancję po nazwie lub numerze UN i w jej opisie znaleźć informację o ograniczeniach sorbowania (Potentially Incompatible Absorbents).
Jeżeli nadtlenek organiczny chcemy poddać neutralizacji w miejscu bezpiecznym lub przeprowadzić dekontaminację terenu z wykorzystaniem neutralizatora, musi się to bezwzględnie odbywać pod nadzorem eksperta.
Proces neutralizacji nadtlenków organicznych dokonuje się w środowisku zasadowym. W przypadku nadtlenku benzoilu wykorzystuje się 10% roztwór NaOH, aplikując jego około czterokrotnie większą masę, niż wynosi masa nadtlenku. Reakcja jest w bardzo nieznacznym stopniu egzotermiczna, więc nie wymaga chłodzenia. Do neutralizacji należy wykorzystywać roztwór o temperaturze nie wyższej niż 25oC. Przy ciągłym mieszaniu składników czas hydrolizy w tych warunkach będzie wynosił około 3 godz. Należy pamiętać, by wszystkie operacje przeprowadzać na zwilżonym nadtlenku, chyba że formulacja jest zawiesiną wodną.
Podobnie przebiega np. neutralizacja nadtlenku ketonu metylowo-etylowego rozpuszczonego we ftalanie dimetylu. W tym przypadku warto zastosować bardziej stężony 20% roztwór NaOH w stosunku masowym względem formulacji nadtlenku 10:1.
Przypisy
[1] James H. Meidl, Explosive and toxic hazardous materials, Glencoe Press, 1970.
st. kpt. dr Tomasz Węsierski pełni służbę w Instytucie Inżynierii Bezpieczeństwa SGSP
